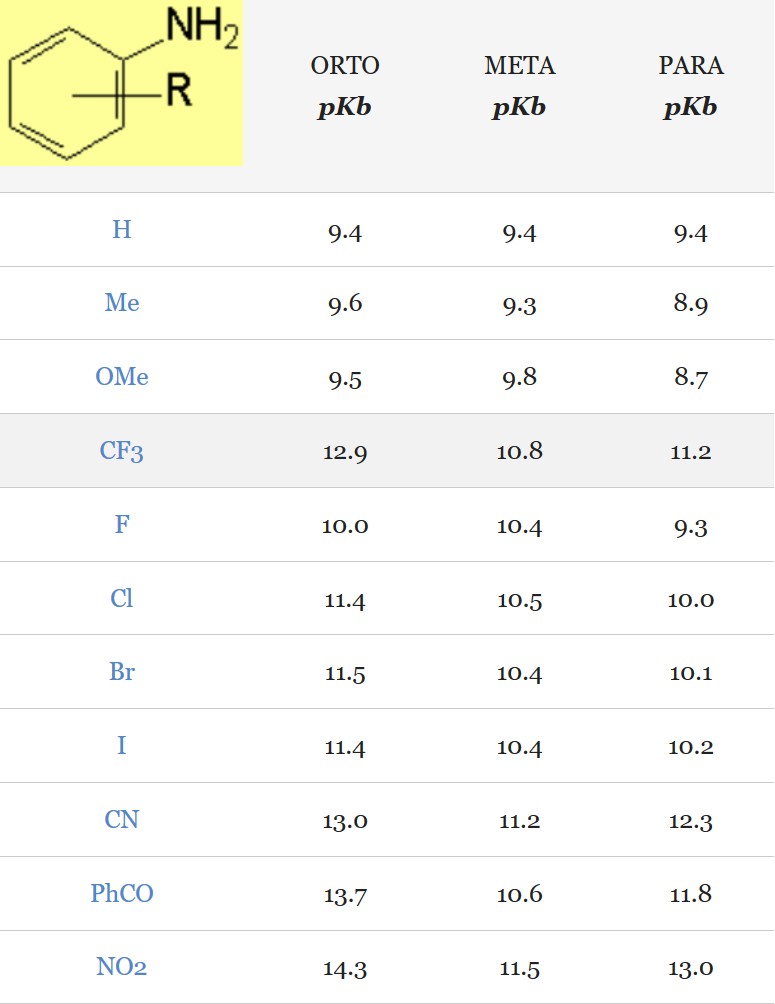

El grupo CF3 aumenta el pKb de la anilina, con lo que la hace menos básica. El grupo CF3 hace que el par de electrones del nitrógeno esté menos accesible a un ácido externo. La disminución de basicidad ocurre el orden orto > para > meta.
El grupo CF3 es muy electronegativo por la presencia de los tres átomos de flúor. El que la disminución de la basicidad sea mayor en las posiciones orto y para no sorprende porque en ellas la transmisión por resonancia de los efectos electrónicos es más eficiente. Podríamos escribir formas resonantes con hiperconjugación para explicar la disminución de la basicidad en la para-trifluormetilanilina.
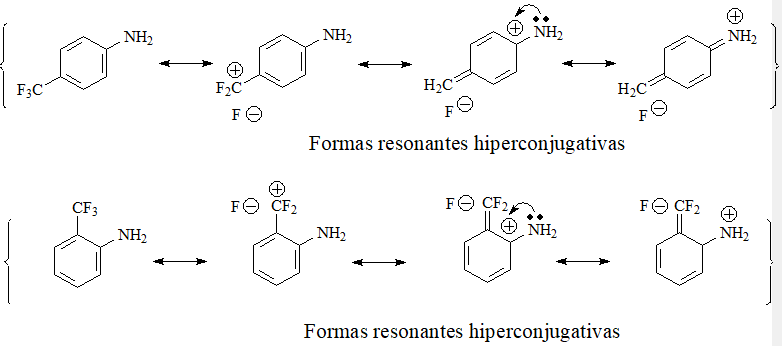
En posición meta la basicidad disminuye, pero no tanto como en para u orto. En meta no puede escribirse una forma resonante similar a las mostradas en orto o para, donde el par de electrones del nitrógeno se deslocaliza hacia el anillo. La menor disminución de la basicidad debe provenir de la expresión exclusiva del efecto de electronegatividad y no del resonante.
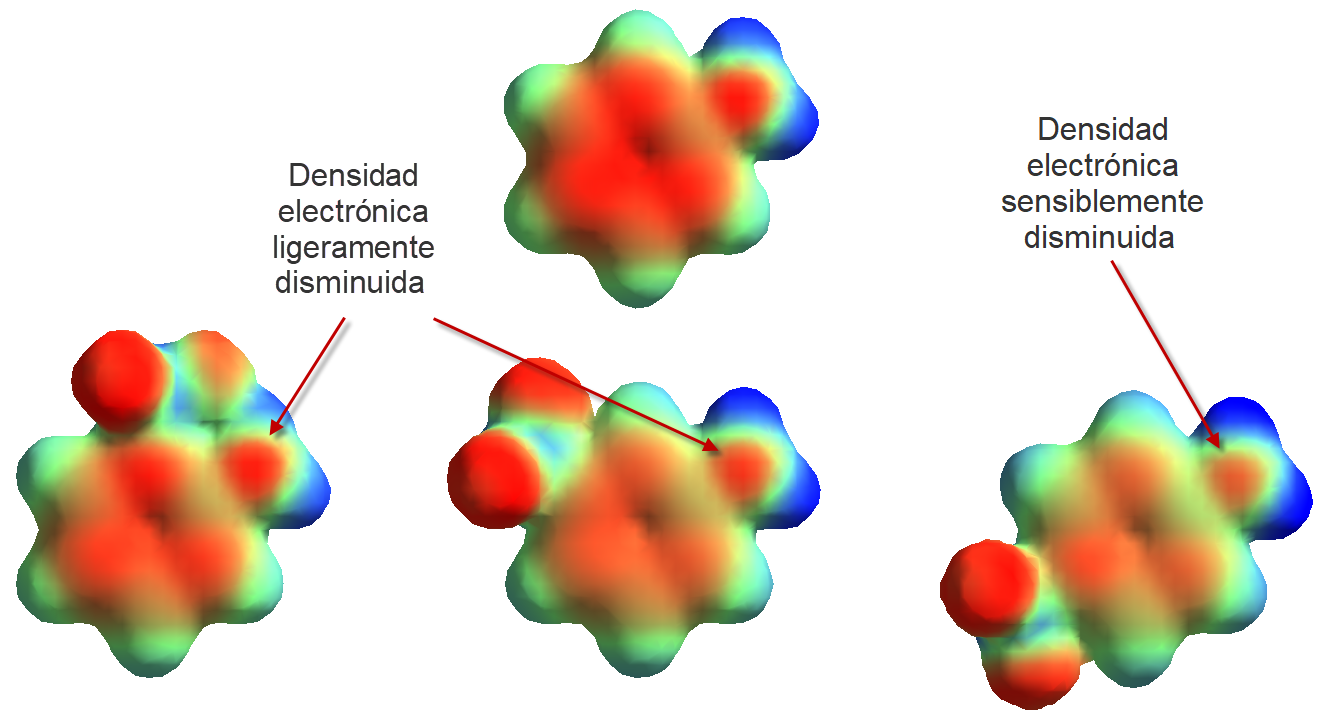
El cálculo de la densidad electrónica permite apreciar diferencias más o menos grandes en la densidad electrónica del nitrógeno, entre la anilina (arriba) y las tres trifluormetilaninilas posibles, que están de acuerdo con las variaciones en los valores de pKb experimentales.